-
中国强之国产疫苗替代,康泰、智飞、沃森能否扛起这杆大旗!
操盘手涛哥111
 / 2019-12-17 21:11 发布
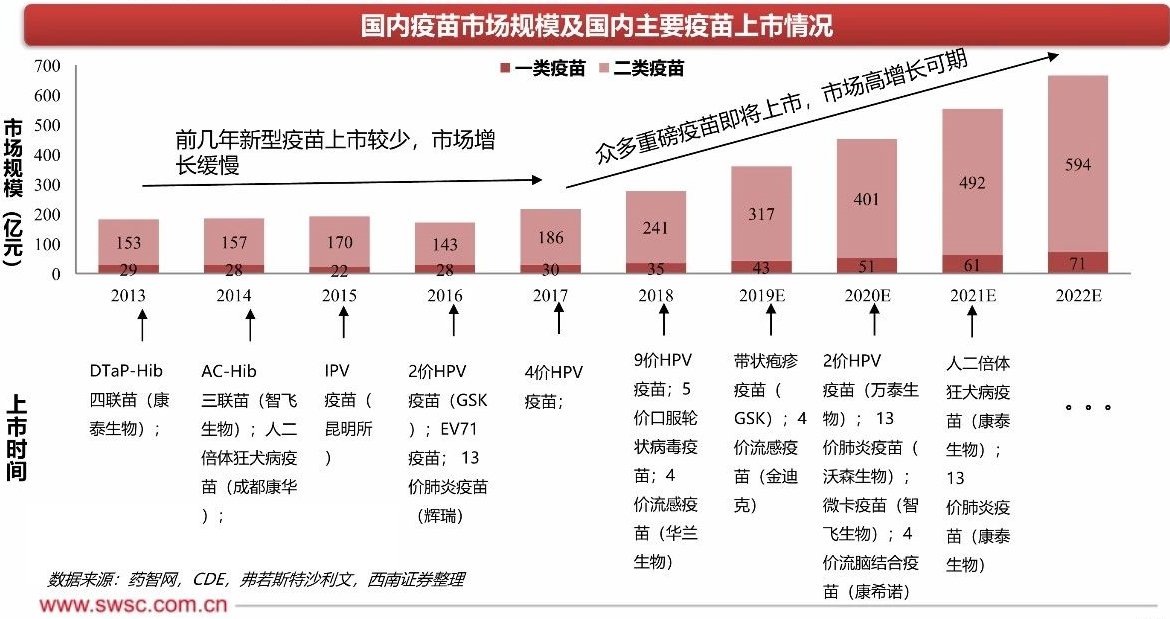
/ 2019-12-17 21:11 发布国产疫苗未来三年拥有众多重磅产品上市,推动行业进一步加速发展,国内人口基数大,市场需求明显,叠加重磅疫苗政策出台,加速行业向龙头公司靠拢,明后年国产13价肺炎疫苗、二倍体狂犬疫苗、EC试剂和结核疫苗等批量上市,相关公司未来成长空间显著增加。重点关注康泰生物、智飞生物、沃森生物。

首先我们先分析第一家,康泰生物,未来疫苗行业的王者
一、公司概况
公司以乙肝疫苗为起点,打造了产品丰富的疫苗梯队。1992 年公司前身康泰有限成立,承接世界疫苗巨头默克的重组乙型肝炎疫苗(酿酒酵母)的全套生产线,1998 年乙肝疫苗获国家药监局正式批准。2002 年公司整体变更为康泰生物,2008年战略重组收购北京民海,并于之后进军麻风联合、四联苗等多联疫苗。2017 年公司在创业板上市,并快速推进 23 价肺炎疫苗、13 价肺炎疫苗、冻干人用狂犬病疫苗(人二倍体细胞)的研发生产进程。我们认为,康泰生物经多年发展已成为研发品种齐全、产品线丰富的疫苗龙头企业。
公司上市至今推行了两次股票期权激励计划,2017 年限制性股票激励计划共授予 175 人首期及预留限制性股票共1233 万股(未复权);2019 年股权激励计划拟授予股票 3500 万股(未复权),其中首期覆盖面扩大至 548人,占公司 2018 年员工总人数比例 47.8%。除 2 名高管外其他 546 名核心管理、技术、业务人员平均每人授予5.77 万股(前复权),考虑授予价格为 45.06 元(前复权),截至 2019 年 9 月 30 日人均浮盈 168 万元,激励力度充分。我们认为,2019 年激励方案公司层面考核要求不高,旨在让员工共享公司高速发展的效益,此次激励有利于激发核心业务骨干的积极性,上下一心促进公司长远发展。
二、疫苗行业趋势
近十年来全球疫苗市场并购整合不断,制药巨头纷纷通过并购进入疫苗市场,GSK、辉瑞、赛诺菲更是通过频繁并购重组积极补充疫苗产品线。根据辉瑞公司官网,辉瑞 2009 年以 680 亿美元收购惠氏,将 13 价肺炎疫苗收入囊中;根据 GSK 官网,2014 年 GSK 和诺华进行了肿瘤业务和疫苗业务的巨额资产互换,GSK 获得诺华除流感疫苗外的所有疫苗业务;根据赛诺菲官网,赛诺菲于 2017 年斥资 7.5 亿美元收购 Protein Sciences,获得四价流感疫苗 Flublok®……至 2018 年四大疫苗巨头 GSK、MSD、Pfizer、Sanofi合计占全球市场份额 85.3% ,其中 GSK 以 72 亿美元高居榜首。
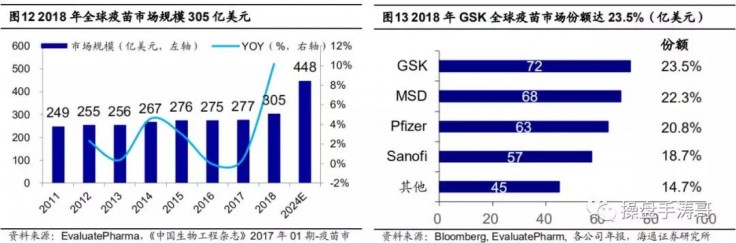
2018 年全球疫苗市场 Top10 销售额合计为 190 亿美元,占全球市场份额达 62.3%,其中 8 个为多联多价疫苗。辉瑞的 13 价肺炎疫苗(Prevnar 13)销售额位居首位,该产品又被誉为 “全球疫苗之王”,2018 年销售额高达58.02 亿美元。默沙东的四价/九价人乳头瘤病毒(HPV)疫苗(Gardasil 4&9)销售额稳居第二位,2018 年销售额高达 31.51亿美元。赛诺菲的百白破-脊灰-Hib 五联苗、四价流感疫苗和默沙东的麻腮风-水痘四联疫苗分别位居第 3、4、5 位。我们认为多联多价疫苗具备简化免疫程序,降低交叉感染及不良反应几率,提高接种率等优点,是未来疫苗的发展方向。

2018 年中国疫苗市场规模预计为 276 亿元,其中公共市场规模为 32 亿元,私人市场规模为 244 亿元,相比公共市场规模为免费向公众提供的疫苗,私人市场疫苗由公众自费购买,定价和利润相对较高,参考 EV71 疫苗、五价轮状病毒疫苗等新型疫苗上市后快速放量,随着 13 价肺炎疫苗、人二倍体细胞狂犬疫苗等新型疫苗陆续面市,将驱动国内疫苗市场高速扩容。
三、公司现有产品
康泰生物已上市疫苗品种为 5 类,涵盖免疫规划疫苗和非免疫规划疫苗。公司目前有五类疫苗上市:重组乙型肝炎疫苗(酿酒酵母)、b 型流感嗜血杆菌结合疫苗、麻疹风疹联合减毒活疫苗、无细胞百白破 b 型流感嗜血杆菌联合疫苗、23 价肺炎球菌多糖疫苗,其中免疫规划疫苗两款:10μg/0.5ml/支乙肝疫苗和麻风二联苗。
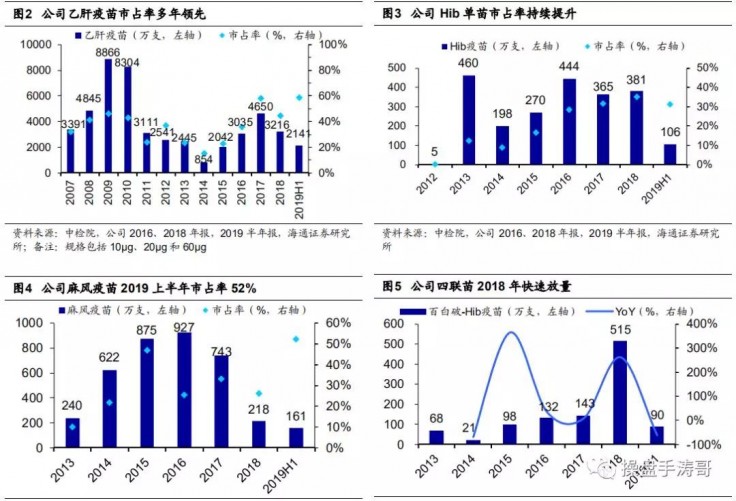
公司独家产品四联苗提高接种依从性。百白破-Hib 四联苗全称“无细胞百白破 b型流感嗜血杆菌联合疫苗”,用于预防百日咳杆菌、白喉杆菌、破伤风梭状芽孢杆菌和 b 型流感嗜血杆菌引起的多种疾病,适用人群为 3 月龄以上婴儿,为全资子公司民海生物国内独家品种。相比百白破疫苗或 Hib 结合疫苗,四联苗可减少注射次
数 4 次。我们预计会提高婴幼儿接种的依从性,四联苗、五联苗等多联苗替代单苗优势明显。
四联苗驱动公司近年业绩高速增长。2018 年公司四联苗收入 11.60 亿元实现超高速增长+182.27%,占疫苗产品总收入 57.60%,第二大品种乙肝疫苗收入 5.17 亿元(YOY+21.04%),占比 25.66%。2018 年公司实现营收20.17 亿元(YOY+73.69%),归母净利润 4.36 亿元(YOY+102.92%),归母扣非后净利润 4.13亿元(YOY+133.93%),主要系四联苗放量驱动。我们预计 2019 年上半年公司营收及净利润同比下降主要因 2018年同期基数较大及批签发进度放缓。
四、重磅疫苗带动公司未来成长
潜力品种 一:PCV13(13价肺炎疫苗)
肺炎球菌性疾病是全球重要的公共卫生问题之一,造成了严重的健康威胁和沉重的经济负担。我们认为疫苗是预防肺炎球菌感染的最有效手段。已上市的疫苗可分为肺炎球菌多糖疫苗和肺炎球菌结合疫苗。13 价肺炎链球菌结合疫苗(PCV13)预防肺炎球菌血清型及适用人群较广泛,2019 年全球 114 个国家将 PCV13 纳入国家免疫规划。考虑到肺炎链球菌的耐药性问题日益严重, WHO 建议全球各国均应将 PCV 纳入本国的儿童免疫接种规划。
沃森生物和康泰生物的PCV13研发进度最快。目前国内有9家公司开展13(15)价肺炎结合疫苗研究。其中沃森生物和康泰生物进度最快,先后进入生产申报阶段,我们判断后续公司13价肺炎有望进入优先审评,预计20年两家公司将有望获批。
康泰13价覆盖到71月龄(辉瑞15月龄以内,2,4,6月龄基础三剂次,12-15月龄加强1次),免疫程序也比辉瑞产品灵活:2月龄4剂次,7-11月龄3剂次;12-35月龄2剂次,2-5周岁1剂次。价格方面,辉瑞原研品种沛儿中标价为698元/支,我们预计公司定价500元/支。仅考虑新生儿增量市场,参考国内2类疫苗Hib相关疫苗市场渗透率30%左右,我们预计PCV-13渗透率有望达30%,国内每年新生儿1500万计算,每年增量市场450万人份,每人份2000元,国内新生儿市场90亿元;内共有5家企业产品进入临床阶段,其中进展最快的是沃森生物,康泰13价预计20年获批,将成为第3家获批上市的企业(包括外资)。兰州所处在3期临床。预计5年内最多3家企业与康泰竞争(包括外资)。假设康泰13价肺炎疫苗国内市场份额25%左右,预计销售收入将突破20亿,有望贡献10亿以上净利润。公司一期产能1000万剂次已建成,考虑到全球市场巨大需求,公司规划了二期产能2000-3000万剂次,预计2-3年内建成。
潜力品种二:HDCV(狂犬疫苗)
人用狂犬病疫苗则主要用于暴露后预防(post exposure prophylaxis, PEP)和高危人群的暴露前,我国人用狂犬病疫苗每年批签发量 1200-1600 万人份,HDCV 份额仅 3%。根据 2016 年国家疾控中心发布的《狂犬病预防控制使用技术指南(2016 版)》,估计全国狂犬病年暴露人口数逾 4000 万。近年来我国人用狂犬病疫苗批签发量在6000-8000 万支左右,按“五针法”算对应 1200-1600 万人份,2018 年 CPRV(包含冻干和非冻干)的批签发份额高达 88%,HDCV 仅有康华生物一家厂商,份额仅为 3%。
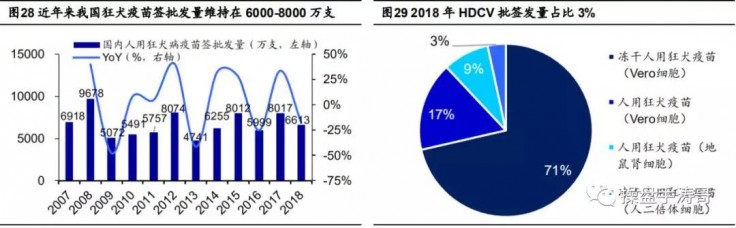
目前国内共有 7 家厂商布局人用狂犬疫苗研发,康泰生物进度最快。北京民海(康泰生物子公司)的冻干人用狂犬病疫苗(人二倍体细胞)已完成Ⅲ期临床研究,公司于 2019 年 8 月收到临床试验总结报告,具备了申报生产的必备条件。根据公司《关于全资子公司撤回药品注册申请的公告》,康泰生物的该产品是在从巴斯德引进冻干人用狂犬疫苗(MRC-5 细胞)基础上进行工艺优化的项目,具有生产工艺先进、质量稳定、生产成本低等优势,并大幅降低了后续向巴斯德支付的技术许可使用费。其他 6 家厂商如辽宁成大、昆明所等均处于临床批件阶段,尚处于早期。
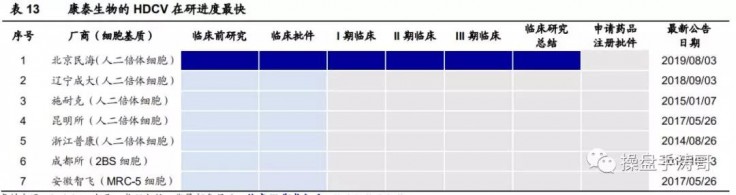
目前 HDCV 国内厂商仅康华生物一家,产能 300 万支较低,2018 年批签发量近 210 万支,占狂犬疫苗批签发量仅 3%。康华生物目前 HDCV 单支定价 266 元,相对国外上市 HDCV——巴斯德的Imovax 380 美元的单支定价较低,但高于国内 CPRV 单支约 55 元的定价。我们预计康泰生物的 HDCV 于 2021 年上市销售,随着两家厂商共同开发市场,HDCV 的渗透率逐渐提升至 20%,康泰生物的 HDCV 凭借生产成本低、销售能力强等优势迅速提升市占率,预计 2024 年公司 HDCV 可达 18 亿元的峰值销售额。
潜力品种三:IPV(脊灰疫苗)
我国 IPV 批签发量随着国产品种上市而迅速增长,2016 年 5 月,我国实施新的脊灰免疫策略,在常规免疫中停用 tOPV 并启用 bOPV。脊灰疫苗接种为 1 剂 IPV+3 剂 OPV。2009年巴斯德的 IPV在国内获批上市,国产厂商昆明所和北生研的 IPV分别于 2015年 1 月和 2017 年 8 月获批,2018 年我国 IPV 批签发量达到 3301 万支,占脊灰疫苗批签发总量的 19.3%。
目前国内 IPV 获批厂商为昆明所和北生研,其中昆明所正在补充临床 IV 期实验。科兴生物已完成 III 期临床试验并报产,武汉所 III 期已招募完成,康泰生物正进行临床 III 期招募,北京天坛生物正处于临床 I 期试验阶段。
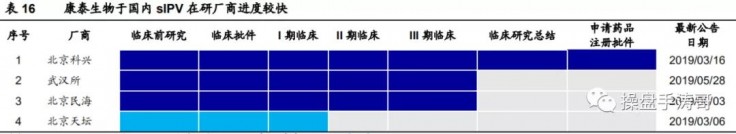
2018 年国内 IPV 批签发量为 3301万支,仅考虑新生儿市场其接种率高达 54%,IPV 目前单支定价 168-178元,随着更多企业 IPV 产品获批,我们保守预计单支定价下降至 100 元,则对应市场规模超 50 亿元。我们预计康泰生物的 IPV 于 2022 年上市销售,峰值市占率 20%对应销售额 11 亿元。
潜力品种四:EV71(手足口)
2008-2015 年我国共报告 HFMD 约 1380 万例,平均年发病率为 147/10 万,报告重症病例约 13 万例,死亡3300 多人,严重威胁了我国儿童的生命健康,我国手足口病多发,目前尚无特效抗肠道病毒药物。疫苗接种是预防 EV71 感染的有效措施。EV71 疫苗可用于 6 月龄-5 岁儿童预防 EV71 感染所致的手足口病,昆明所和科兴生物的 EV71疫苗于 2015 年 12 月获批上市,2016 年 12 月武汉所的 EV71 疫苗获批,为预防EV71 感染和HFMD 提供重要手段。
昆明所、武汉所和北京科兴生物产品已上市销售,其中昆明所已完成临床 IV 期试验;武汉所和北京科兴生物处于临床 VI 期观察阶段;北京民海(康泰生物子公司)正处于临床 II 期阶段;康泰生物 EV71 疫苗系由重组汉逊酵母表达的 EV71 抗原经纯化加入铝佐剂制成,是以基因工程技术为基础进行的研究,与传统灭活疫苗和减毒活疫苗相比,安全性更高并更适合大规模生产。
目前 EV71 疫苗单支定价168-198 元,我们预计于 2022 年随着康泰生物加入市场单支定价回落至 150 元,
则 2022-2025 年预计国内新生儿 EV71 疫苗市场规模 22.5 亿元。假设 2025 年康泰生物达峰值市占率20%,对应峰值销售额为4.5亿元。
五、盈利预测
我们预计公司 2019-2021 年归母净利润为 5.41、7.54、11.74 亿元,同比增长24.15%、39.44%、55.65%,对应 EPS 为 0.84、1.17、1.82 元。公司在研疫苗储备丰富,全球销售额 Top10 品种已布局 8 个,PCV13、HDCV 等重磅品种上市后将助推公司业绩腾飞。
公司未来成长可期,但现在估值较高,两款重磅疫苗大概率明年下半年开始量产,业绩有望在2021年开始释放,对于长期投资来说,明显年中左右应该是个不错的时间选择。
风险提示:疫苗行业负面事件风险,研发进度低于预期风险,疫苗产品销售不达预期风险,
本文由以下信息整理采编:《海通证券:康泰生物——研发管线迎来收获,重磅品种呼之欲出》
2、智飞生物
智飞生物自 2002 年进入疫苗行业,早期以疫苗代理为主,经过多年的自主研发投入,逐步形成以自营自销自主产品为基础,以代理销售进口优质疫苗为延伸的业务格局,是我国综合实力最强的民营疫苗企业之一。
公司股权结构集中,董事长兼总经理蒋仁生先生持股 53.13%,公司现有五家全资子公司及一家参股子公司,其中智飞绿竹是以预防脑膜炎、肺炎为主的细菌性疫苗产品平台;智飞龙科马是防治结核类生物制品及预防狂犬病毒、流感病毒等病毒类疫苗产品平台;智飞空港为公司代理产品提供进口和仓储服务;重庆智仁主要从事普通药品销售;智飞互联网主要从事互联网技术开发、目前尚未发生实际经营活动;
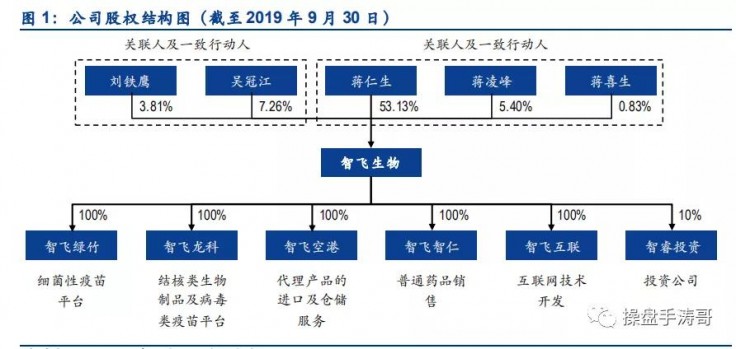
公司主营业务主要包括自主产品与代理产品两大部分。自主产品包括二类疫苗(AC 流脑结合疫苗、Hib 疫苗、ACYW135 流脑多糖疫苗及 AC-Hib 三联苗)与治疗性生物制品(注射用母牛分支枝菌,简称微卡);代理产品以默沙东的疫苗为主,包括四价 HPV疫苗、九价 HPV疫苗、五价轮状病毒疫苗、甲肝灭活疫苗及 23 价肺炎多糖疫苗;此外,公司还为浙江普康的冻干甲肝减毒活疫苗提供市场推广服务。
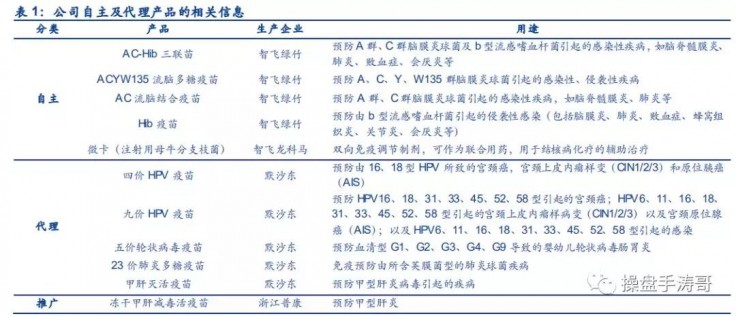
公司现有 2 个研发基地、1 个研发中心,通过自主研发构建了行业领先的研发管线。目前公司在研项目达 22 项,涉及流脑、肺结核、肺炎、流感、狂犬病等人用疫苗项目建设。其中,预防微卡与 EC 诊断试剂已申报生产,并预计有望 2020 年初获批上市;三价流感疫苗已完成临床试验,预计有望近期申报上市;四价流感疫苗与 23 价肺炎多糖疫苗正处于 III 期临床阶段,预计有望 2021-2022 年获批上市;狂犬疫苗(MRC-5 细胞)已登记 III 期临床,15价肺炎结合疫苗已登记 I 期临床、即将开展 III 期临床,预计有望 2022-2023 年获批上市。
一、自主研发疫苗:预防微卡上市在即,15 价肺炎疫苗值得期待
1、预防微卡
结核病是全球十大死因之一,也是最大的单一感染性病原体致死原因(高于艾滋病),每年有数百万人罹患结核病。按照世卫组织 2017 年数据,中国结核病发病人群排在全球第二位,近年每年发病病人在 80 万人以上。WHO 期望在 2035 年终止结核的流行,发病率和死亡率分别要降 90%、95%,2011 年卫生部发布的全国第五次结核病流行病学调查结果显示,中国感染肺结核病菌人群约为 5.5 亿人,占全国总人数的45%。2018 年我国肺结核发病人数 88.9 万人,死亡人数 2823 人,结核病发病人数仍然较多,中西部地区、农村地区结核病防治形势严峻。
对于当前国内结核病预防而言,形势严峻,在预防和大规模筛查端都处于缺失状态,首先没有有效的大规模筛查手段,一般的 PPD 方法假阳性过高,γ干扰素方法成本则太高,因此无法有效筛选出带菌人群;其次即使带菌人群筛选出来,也没有有效的预防手段,目前国内乃至世界并无有效的成人结核预防疫苗。而智飞的 EC 诊断试剂和预防用母牛分歧杆菌疫苗恰恰可以解决这两个方面的空缺。
公司研发的结核菌筛查用“重组结核杆菌 ESAT6-CFP10 变态反应原”IGRA 法结核诊断试剂(EC 试剂)目前已完成 III 期临床,目前已申报生产,处于审批尾声。与目前特异性高、WHO 推荐的 IGRA 法相比,成本低、特异性相当,此试剂的上市将大幅改善结核菌高危人群筛查的便利程度与成本,提高筛查普及率与预防性治疗参与度,为结核疾病的大规模筛查提供可能。目前龙科马的“重组结核杆ESAT6-CFP10 变态反应原”产业化项目已初步完成,未来可生产 EC 结核诊断试剂预计在 2000 万剂/年,未来还有望进一步扩大产能。
预防性微卡是全球唯一进入临床 III期并且申报生产的结核疫苗,为原治疗性微卡的适应症拓展项目,主要用于 15-65 岁结核菌素纯蛋白衍生物(TB-PPD) 皮肤试验强阳性患者,公司目前已完成临床三期,在最后的审评阶段,根据审评进度,我们预计2020年一季度内有望获批上市。随着预防性微卡的获批,将有效解决国内在结核带菌人群的预防空缺,在结核病的预防端搭起坚固的防线。
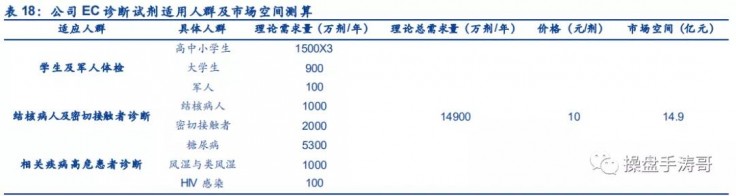
根据公司可行性研究报告披露数据,EC 诊断试剂将主要用于:
1)学生入学及军人入伍体检:我国每年分别有约 1500 万小学、初中、高中学生和约 900 万大学生入学以及约 100 万军人入伍,这部分人群的入学或入伍体检的刚性需求为 5500 万剂。
2)结核病人及密切接触者诊断:国内有 450 万结核病患病人和每年 90 万新发病人,其在出入院时均需进行结核菌感染的诊断,刚性需求约 1000 万剂;据此每年还有约 1000 万结核病密切接触者,理论需求为2000 万剂。
3)相关疾病高危患者诊断:结核病与糖尿病、风湿与类风湿、HIV 感染等疾病高度相关,目前国内糖尿病确诊患者约 5300 万人、风湿和类风湿患者将近 1000 万人、HIV感染者约 100 万人,这部分人群的理论需求为 6400 万剂。综合测算,我国 EC 诊断试剂的每年理论需求预计超过 1.5 亿剂。
根据现有国家政策推测,由于我国结核病防治形势严峻,公司 EC 诊断试剂有望大概率获得国家统
一集中采购,哪怕按 10 元/剂的价格保守计算,公司 EC 诊断试剂的市场空间也将达到 15 亿元。
预防微卡的适应人群为结核杆菌潜伏感染人群,因此预防微卡的接种应以 EC 诊断试剂筛查为前臵条件。仅考虑每年新入学学生、入伍军人等刚性筛查人群,假设我国真正潜伏感染比例为 20%,导流接种比例为 20%-40%,则对应预防微卡的接种人群为 220万-440 万人。根据公司公告及公开调研信息,公司预防微卡预计定价 300-400 元/针,接种程序 6 针/人,据此测算,预防微卡市场空间为 46-92 亿元。
目前资本市场对预防微卡尚未形成充分认识,或对其市场推广与销售放量存在一定疑虑,市场预期差较大;但我们认为,在国家政策导向下,EC 诊断试剂筛查为预防微卡接种建立了良好的前臵导流条件,预防微卡未来市场放量确定性较强。根据 DCF 估值模型,我们预计公司预防微卡经风险调整后的净现值为 148.7 亿元。
2、15价肺炎疫苗
2018 年全球已有 144 个国家将肺炎结合疫苗纳入免疫规划,15 个国家计划将其纳入免疫规划。13 价肺炎结合疫苗凭借其多价、高保护率、全年龄覆盖等优势,在全球市场中占据主导地位。根据 IVAC 数据,目前全球 144 个将肺炎结合疫苗纳入免疫规划的国家中,106 个国家选择使用 13 价肺炎结合疫苗,30 个国家选择使用 10 价肺炎结合疫苗,另有 8 个国家同时使用 10 价和 13 价疫苗。
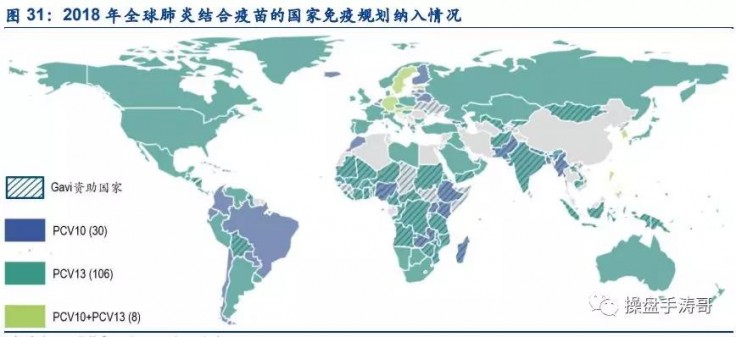
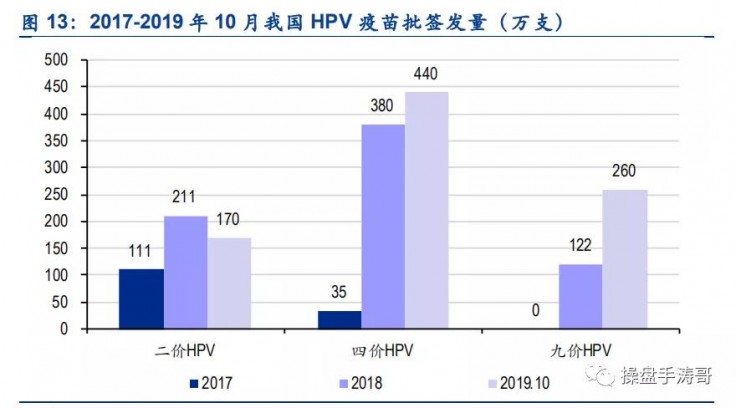
我国每年约 174 万名儿童发生严重的肺炎球菌感染,其中死亡人数达 3 万人,2016 年 11 月,辉瑞 13 价肺炎结合疫苗在我国获批上市,2018 年批签发量达到 385 万支。以新生人口 1523 万,接种程序为 4 支/人份测算,2018年我国 13 价肺炎结合疫苗的市场渗透率仅 6.3%,远不能满足国内市场需求。同时,考虑到13 价肺炎结合疫苗已被全球 114 个国家纳入免疫规划,辉瑞须优先满足这些国家的疫苗需求,因此我们预计,辉瑞对我国的 13 价肺炎结合疫苗供给有限(2019 年 1-10 月份批签发量仅 288 万支)。
参考国内系列疫苗接种率,我们预计,未来国内适龄儿童的肺炎结合疫苗接种率有望达到20%-40%。按我国每年新生人口 1500 万,平均中标价 600 元/支,接种程序为 4 支/人份测算,国内肺炎结合疫苗的市场空间达 72-144 亿元。
我国多家企业正在开展肺炎结合疫苗的研发工作,但研发品种主要集中于 13 价肺炎结合疫苗,其中沃森生物与康泰生物的研发进度较为领先。沃森生物于 2018年 2 月申报生产,并于 2018 年 4 月被纳入优先审评,预计 2020 年初获批上市;康泰生物已提交药品注册批件预申请,有望在 2020 年获批上市。而对于更高价肺炎结合疫苗,只有公司研发的 15 价肺炎结合疫苗已获批临床,并于 2019 年 6 月进入 I 期临床阶段、即将开展III 期临床。

3、其他品种
其他品种方面,公司的四价流感疫苗、23价肺炎多糖疫苗、三代狂犬疫苗都已经进入三期临床,未来随着获批生产,带来自研产品将进一步增加公司长期收益。
二、代理品种:HPV 销售持续高增长,五价轮状市场替代可期
1、HPV 疫苗
宫颈癌是致死率仅次于卵巢癌的女性生殖道恶性肿瘤,我国妇女患宫颈癌的比例为 15/10 万,是仅次于智利的全球第二大宫颈癌高发国家,人乳头状瘤病毒(HPV)与宫颈癌之间具有高相关性,HPV 感染非常普遍,HPV16、18 是最主要的高危型 HPV,70%的宫颈癌都是由这两种 HPV 亚型导致。
HPV 疫苗是全球第一个用于预防肿瘤的疫苗,预防效果显著且相对安全。其中,一项九价 HPV 疫苗与四价 HPV 疫苗的非劣效试验表明,四价和九价 HPV 疫苗的血清阳转率均接近 100%,抗体应答水平是自然感染的数倍。
目前,全球上市的三种 HPV 疫苗均已在国内获批上市,其中默沙东四价和九价 HPV疫苗的国内销售由公司独家代理,2018 年 11 月,公司与默沙东签署 HPV 疫苗相关协议,在维持协议期限不变(至 2021 年 6月 30 日)的情况下,进一步调整和确定了公司所代理的 HPV 疫苗的综合基础采购额,
2019-2021 年 HPV 疫苗综合基础采购额分别为 55.07 亿、83.30 亿、41.65 亿元。
在当前国内市场教育充分、适龄女性接种高涨的背景下,疫苗供给成为决定公司代理 HPV 疫苗销售放量的核心因素,而随着默沙东分装线的扩产完成,公司代理 HPV 疫苗的 2020 年供给有望明显提升。,公司代理 HPV 疫苗在未来 3-4 年将继续独占国内高价 HPV 疫苗市场,充分享受国内巨大的 HPV 疫苗存量市场红利。
2. 五价轮状疫苗:
人类轮状病毒(HRV)是导致全球儿童急性重症腹泻的主要原因,我国已将轮状病毒腹泻列为国家重点防治的“小儿四病”之一,目前国际市场以 GSK 生产的单价轮状病毒疫苗 和默沙东生产的五价轮状病毒疫苗为主,我国兰州所生产的单价轮状病毒疫苗罗威特及越南 Polyvac 公司生产的Rotavin-M1 疫苗均仅在本国销售。
默沙东五价轮状病毒疫苗RotaTeq 于 2018 年 4 月在国内获批上市,并于 2018 年 9 月首次批签发。公司作为默沙东在中国大陆市场的市场推广服务方,独家进口、推广、经销和销售五价轮状病毒疫苗 RotaTeq,协议期限为 2018 年 7 月 9 日至 2021 年 12 月 31 日,2018-2021 年基础采购计划额分别为 2.47亿、6.5 亿、9.49 亿和 13 亿元。与 HPV 疫苗代理协议类似,公司同样明显上调了五价轮状病毒疫苗 RotaTeq 的基础采购额,彰显出公司对五价轮状病毒疫苗 RotaTeq 国内市场空间及销售快速放量的信心。
3、其他品种
除 HPV 疫苗和五价轮状病毒疫苗外,公司还代理默沙东的 23 价肺炎多糖疫苗和甲肝灭活疫苗2017 年 4 月,公司与默沙东续签疫苗经销与推广服务协议,继续负责默沙东 23价肺炎多糖疫苗和甲肝灭活疫苗在中国大陆市场的推广工作。协议约定,2017-2020 年公司产品采购总额为 2.03 亿、2.54 亿、2.52 亿及 1.90 亿元,推广服务费为 0.62 亿、0.66 亿、0.74 亿及 0.75 亿元。
三、盈利预测及风险提示
1)现有自主品种:虽然三联苗再注册短期遭遇挫折,但看好其长期多联替代市场空间,采用相对估值法,给予公司现有自主品种 35 倍估值;按公司 2019-2020 年净利润分别为 4.1亿、2.6 亿元测算(剔除预防微卡及 EC 诊断试剂利润),对应 2019-2020 年合理市值分别为144 亿、91 亿元;
2)现有代理品种:考虑到 HPV 疫苗及五价轮状疫苗市场竞争格局良好、市场需求旺盛,同时公司与默沙东大概率续签代理协议,采用相对估值法,给予公司现有代理品种 25 倍估值;按公司 2019-
2020 年净利润分别为 19.9 亿、30.7 亿元测算,对应 2019-2020 年合理市值分别为 498 亿、768 亿元;
3)在研品种:根据 DCF 模型测算,我们认为,公司在研预防微卡与其他品种的 2019年合理市值分别为 149 亿和 50 亿元,2020 年合理市值分别为 200 亿和 60 亿元,不考虑其他早期在研品种,公司研发管线的 2019-2020 年合理市值分别为 199 亿、260亿元
据此测算,公司 2019-2020 年合理市值分别为 841 亿、1119 亿元。
风险提示:疫苗安全事故风险、疫苗研发不及预期、三联苗再注册不通过风险等
3、沃森生物
公司创立于 2001 年,于 2010 年 11 月在创业板上市,公司以传统疫苗起家,后通过外延收购上海泽润、嘉和生物(目前已变为参股),逐渐向新型疫苗、单克隆抗体领域发展。根据药监局网站进度,13 价肺炎多糖结合疫苗目前已进入生产审批的最后阶段,上市时间预计在年内。13 价肺炎多糖结合疫苗 2018 年全球销售规模 58 亿美元,是当之无愧的疫苗销售之王,我们认为 13 价肺炎疫苗未来上市后将大超市场预期,为公司带来巨大的业绩增量;另外子公司上海泽润的二价 HPV 处于临床 III 期收尾阶段,国内市场潜在需求人群巨大,有望于 19 年内揭盲。
1、13 价肺炎多糖结合疫苗
13 价肺炎多糖结合疫苗被称为全球“疫苗销售之王”,由辉瑞公司独家生产,目前已进入全球 100 多个国家的免疫规划当中,13 价肺炎结合疫苗是目前唯一一款用于全年龄组人群注射的肺炎疫苗,是全球使用最为广泛的肺炎球菌多糖结合疫苗。18 年全球销售58 亿美元,继续强劲势头。
国产 13 价肺炎疫苗沃森生物和康泰生物处于领先地位,相关进展将成为疫苗板块第二波浪潮的巨大催化剂。按照当前的研发进度,沃森生物于 2018 年 3 月份获得优先审评,经过两次资料的发补,根据药监局网站显示进度,我们预计公司产品将于2020 年上市销售;康泰生物目前进展来看,目前已取得临床总结报告,根据药监局网站进度,预计将于 21 年初的时间获批。

预计公司 13 价肺炎结合疫苗上市后将快速放量:鉴于国内强大的市场需求、消费升级属性,上市销售后公司业绩将会获得爆发性成长。按照目前疫苗大产品的销售趋势,我们认为新时代下,13 价肺炎的销售空间有望大超市场预期,我们预计 19-21 年 13 价肺炎的销售情况如下,假设单支价格 550 元左右,50%的净利润率:

二、HPV 疫苗
根据 2015 中国癌症统计报告显示,在女性特有的肿瘤发病率中,宫颈癌位居第二,仅次于乳腺癌,是最常见的妇科恶性肿瘤。2015 年国内宫颈癌新发病例预计在 9.89 万例左右,约占世界新发病例总数的 1/5。2015 年宫颈癌死亡人数 3.05 万例。考虑到缺乏筛查和治疗的人群,实际患者数应高于统计数据。近10年来,宫颈癌的发病率呈上升和年轻化趋势。据资料,目前宫颈癌平均发病年龄由20 年
前的 54 岁,提前到 45 岁。
国内市场空白,消费者呼吁多年,直到 2016 年 7 月 Cervarix 才获得 CFDA批准,而在 17 年 5 月默沙东的四价 Gardasil 也获得 CFDA 批准,国内持续多年的 HPV疫苗空白期已经结束,目前 GSK 和默沙东的 HPV 疫苗(智飞生物独家代理)均已上市销售。多年的市场呼吁也形成了良好的消费者教育效应,为产品上市后的迅速放量垫定了良好的基础。
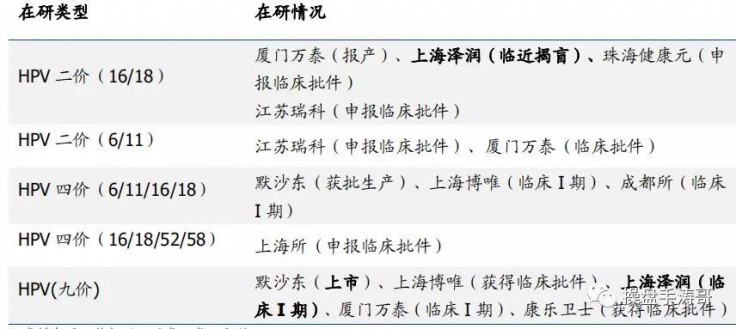
国内产品布局厂家较多,沃森处于领跑地位。沃森生物 2 价 HPV 临床进度领先,公司和厦门万泰属于国内领跑阶段,二者上市时间相差不大,其他厂家布局相对较晚。沃森生物 2 价 HPV 疫苗目前处于临床 III 期后期,妇科随访病例收集阶段,我们预计公司将于 19 年年内揭盲,未来 HPV 疫苗有望放量增长,公司目前的九价 HPV 也已进入临床 I期.
公司作为盖茨基金会国内认可并资助的唯一民营企业,未来在二价 HPV 疫苗和 13 价肺炎结合疫苗上市后将为国际市场提供疫苗帮助。同时大规模的疫苗出口恰恰考验的也是公司在产业化方面的能力。公司在具备研发实力和执行力的同时,产业化的突出优势也进一步提升了企业的市场竞争力。尤其在上市许可人制度全力推行的当下,代工生产受制于他人必然提高企业的生产成本,公司在此方面的提前准备也为未来发展垫定了良好基础。公司目前已经在云南玉溪进行了产业化的铺设:目前 13 价和 HPV 的产业基地都已完成,获得批文后马上可以生产上市,目前产能我们预计较为充足,鉴于国际市场所需产能巨大,我们认为公司未来仍将会有扩产准备;预计 HPV 产能也将保持充足供应,未来同样我们认为基于国际市场的巨大需求,公司仍将有扩产准备。
三、盈利预测
预计公司 19-21 年归母净利润分别为 3.99亿元、13.01 亿元以及 18.14 亿元,对应 PE 分别为 104X、32X 以及 23X;EPS 分别为0.26 元、0.85 元以及 1.18 元。

历史文章:
新能源领域
消费电子
鹏辉能源--动力电池市占率不断提升,TWS 耳机电池快速增长
生物医药
希望大伙儿不要吝啬,动动小手,为涛哥点亮右下角“在看”。每位亲粉都不再冷漠,您的每一份支持对我都至关重要。这是你我互动的信号,每一个赞都会让我格外暖心。
大伙儿快快行动起来,点点赞,鼓励我继续为大伙儿更新最前沿的投研认知,点击“再看”超过5次,可以单独私信领取最新研究成果!!!
予人玫瑰,手有余香。
水晶球APP
高手云集的股票社区
X





 公安备案号 51010802001128号
公安备案号 51010802001128号